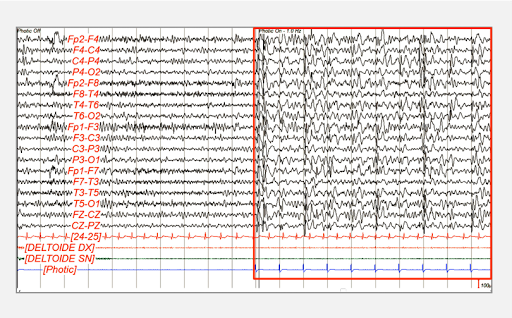
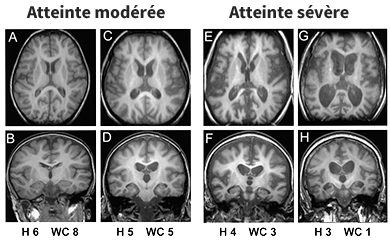
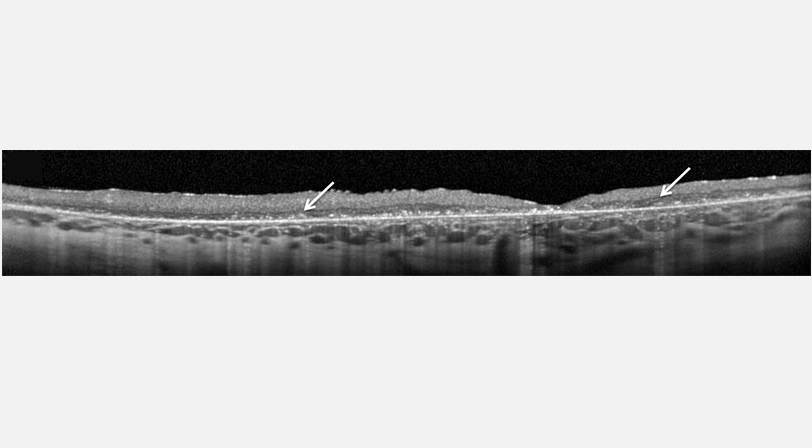
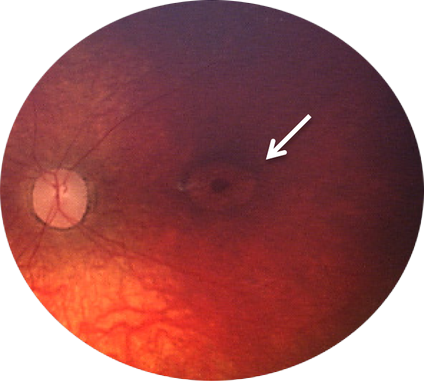
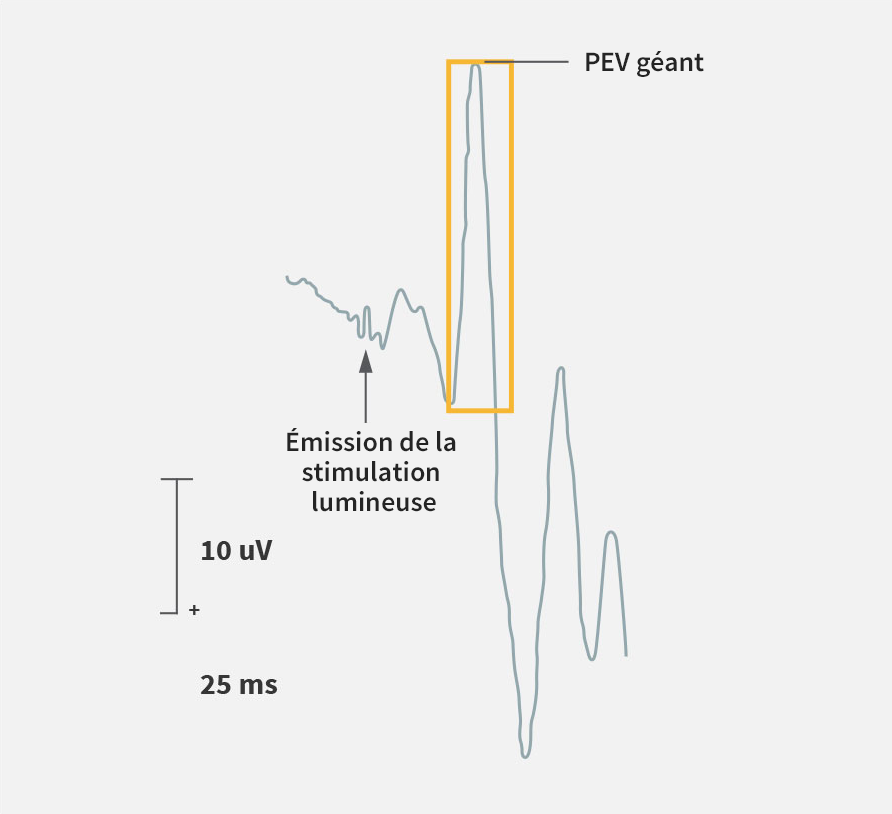
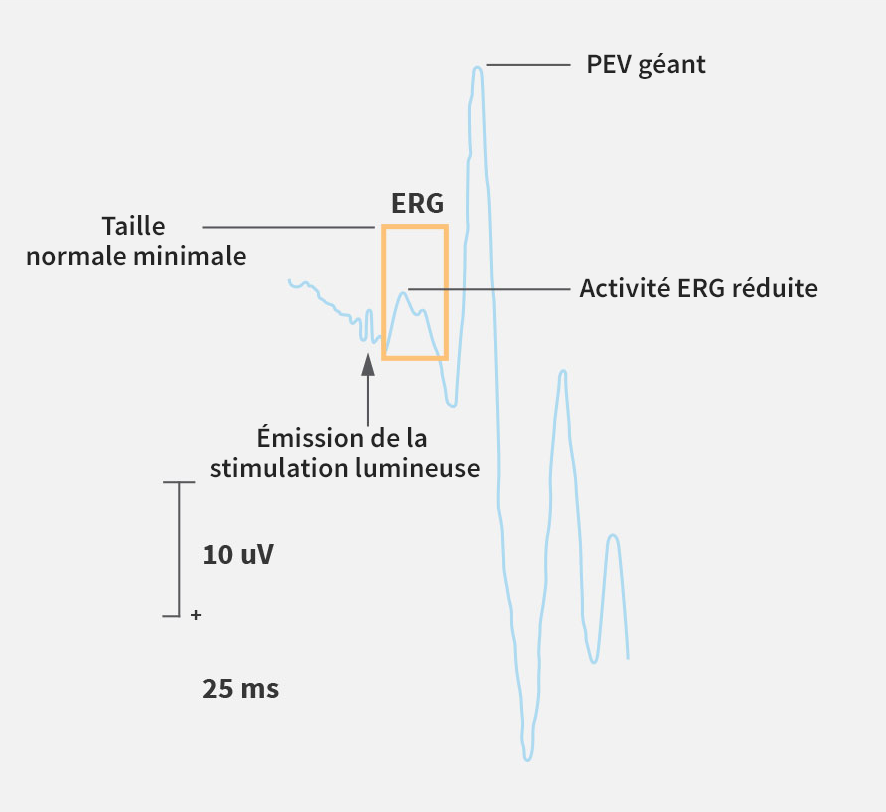
Évaluations cliniques
Références : 1. Chang M, Cooper JD, Davidson BL, et al. CLN2. In: Mole S, Williams R, and Goebel H, eds. The neuronal ceroid lipofuscinoses (Batten Disease). 2nd ed. Oxford, United Kingdom: Oxford University Press; 2011:80-109. 2. Mole SE, Williams RE, and Goebel HH. Correlations between genotype, ultrastructural morphology and clinical phenotype in the neuronal ceroid lipofuscinoses. Neurogenetics. 2005;6:107-126. 3. Albert DV, Yin H, De Los Reyes EC, Vidaurre J. Unique Characteristics of the photoparoxysmal response in patients with neuronal ceroid lipofuscinosis type 2: can EEG be a biomarker? [Epub ahead of print July 21, 2016]. J Child Neurol. DOI: 10.1177/0883073816658659. 4. Fietz M, AlSayed M, Burke D, et al. Diagnosis of neuronal ceroid lipofuscinosis type 2 (CLN2 disease): Expert recommendations for early detection and laboratory diagnosis. [Epub ahead of print July 25, 2016]. Mol Genet Metab. doi: 10.1016/j.ymgme.2016.07.011. 5. Mole SE, Williams RE. Neuronal ceroid-lipofuscinoses. 2001 Oct 10 [Updated 2013 Aug 1]. In: Pagon RA, Adam MP, Ardinger HH, et al., editors. GeneReviews® [internet]. Seattle, WA: University of Washington; 1993-2016. 6. Orlin A, Sondhi D, Witmer MT, et al. Spectrum of ocular manifestations in CLN2-associated Batten (Jansky-Bielschowsky) Disease correlate with advancing age and deteriorating neurological function. PLoS One. 2013;8:e73128. doi:10.1371/journal.pone.0073128. 7. Williams RE, Adams HR, Blohm M, et al. Expert opinion on the management of CLN2 disease. Poster session presented at: The 12th Annual WORLD Symposium; February – March 2016; San Diego, CA.
 Français
Français
 UK (English)
UK (English) Español
Español Italiano
Italiano Deutsch
Deutsch Türkçe
Türkçe Русский
Русский